一、引言
酸抑制剂(ARAs)通过升高胃pH值,从而影响某些口服药物的溶解度和溶出特性。当药物与ARAs联合使用时,其生物利用度可能发生显著改变——对于弱碱性药物可能导致疗效降低;对于弱酸性药物则可能增加不良事件风险。目前临床上广泛应用的ARAs主要包括三类:抗酸药(antacids)、组胺H2受体拮抗剂(H2受体阻滞剂)和质子泵抑制剂(PPIs)。值得注意的是,这些药物既可通过处方获得,也可作为非处方药购买。这意味着,药物与ARAs联合给药存在潜在的临床显著药物-药物相互作用(DDI)风险。鉴于这一风险,在药物研发早期评估研究药物对胃pH变化介导的DDI(称为pH依赖性DDI)的敏感性至关重要。需要时,应通过临床试验明确DDI效应,并在药品说明书中载明相关研究结论及可行的风险管控措施。
此指南描述了FDA关于以下方面的建议:
1. 何时需要进行与ARAs的临床DDI研究。
2. 此类临床DDI研究的设计。
3. 如何解释这些研究结果。
4. 如何在药品说明书中载明相关研究结论。
需要强调的是,指南不涵盖某些ARAs的其他DDI机制,例如弱酸性药物因形成螯合物复合物(如氢氧化铝或氢氧化镁、碳酸钙)导致的吸收减少,以及某些药物因尿液碱化(如碳酸氢钠)导致的肾脏排泄减少。申办方应在药物研发阶段,按需评估此类药物相互作用的临床影响。
二、何时需要进行与ARAs的临床DDI研究
申办方应在药物研发早期,评估该药物发生pH 依赖性药物相互作用的潜在风险,以便更好地指导后续临床试验中药物与ARAs的给药方案,特别是对于那些很大比例患者可能正在服用ARAs的适应症。一般来说,如果确定药物具有pH依赖性DDI的潜力,申办者应进行临床研究以表征ARAs对研究药物药代动力学的影响(参见第三节);或基于体外试验、计算机模拟、临床已有数据,提供充分论据说明该药物不存在 pH 依赖性药物相互作用。
A. 弱碱性药物的速释制剂
已证实存在pH依赖性DDI的药物大多数是弱碱性药物,其固有水溶性较低,无法达到临床给药剂量所需溶解度(即:最高治疗剂量÷250 mL)。研究药物与ARA相互作用的风险可以基于原料药理化性质与制剂溶出曲线分步评估。
图1提供了一个评估弱碱性药物速释制剂与ARAs临床DDI风险的框架示例。申办者如果采用其他策略评估pH依赖性DDI,应咨询适当的审评部门。
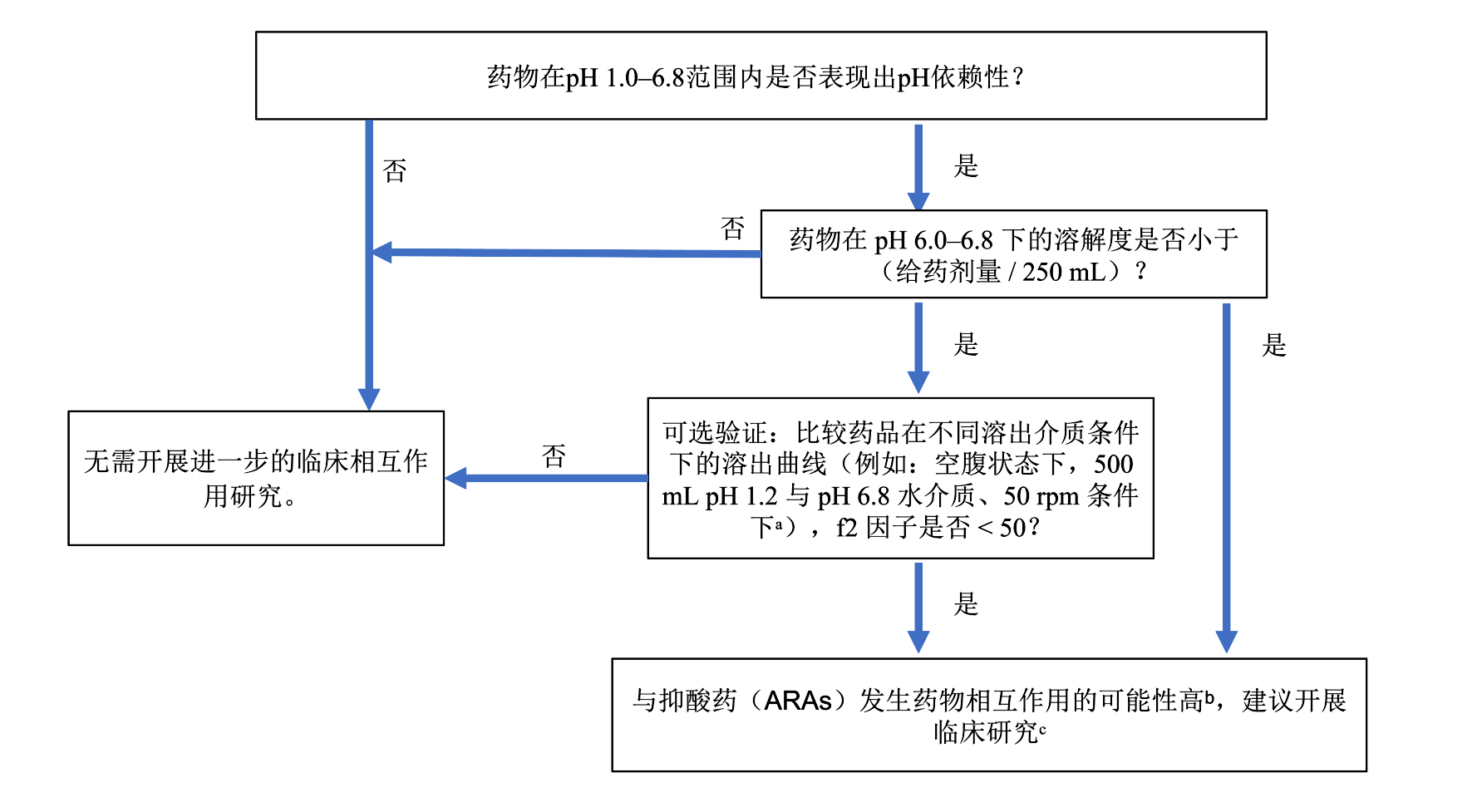 图1. 弱碱性药物速释制剂联用抑酸药的临床药物相互作用(DDI)风险评估框架
图1. 弱碱性药物速释制剂联用抑酸药的临床药物相互作用(DDI)风险评估框架a. 若适用且有合理依据,可结合原料药和制剂的性质,选择其他溶出度参数(如仪器类型、转速)及生物相关介质
b. ARA)存在时,试验药物的平均血药浓度 - 时间曲线下面积(AUC)或血药峰浓度(Cmax)预计降低25% 或以上。该降低幅度对试验药物的临床意义,需基于具体药物的剂量 / 暴露量 - 疗效相关性予以判定。
c. 可考虑采用替代方法(例如群体药代动力学或基于生理的药代动力学建模,详见第四部分)。
f2 – 相似因子;rpm – 每分钟转数
评估时还应兼顾以下额外考量要点:
• 溶解度:
♢ 需明确原料药在生理相关pH范围(例如1.0至6.8)内的水平衡溶解度曲线。
♢ 测定溶解度的pH值宜均匀梯度设置(约一个pH单位梯度),确保能精准表征溶解度曲线的所有拐点。
♢ 由于测量溶解度的溶媒pH可能因供试品药物而改变并偏离初始pH,因此应实测并记录溶液的最终pH。
♢ 用于计算参比溶解度(给药剂量÷250 mL)的剂量应拟定为计划上市的最高治疗剂量。
• 溶出试验所用制剂与给药剂量:
♢ 药物研发早期,可采用初始制剂开展溶出试验,辅助评估在研药物发生pH依赖性药物相互作用的风险。同时,需针对拟上市制剂,按最大治疗剂量完成溶出试验,并完整上报数据。
• 仅在餐后服用的药物:
♢ 胃pH在食物摄入后升高。因此,对于规定餐后服用的药物,应通过比较代表餐后状态pH条件与pH 6-6.8条件下的溶解度和溶出曲线来评估胃pH变化的影响。例如,pH 4-5近似于高脂高热量餐后的pH条件,而清淡餐后胃pH约为2~3。然而,基于体外pH-溶解度和-溶出曲线评估pH依赖性DDI风险存在局限性,因为进食还会促进胆汁酸分泌,进而提升药物在胃肠道内的溶解度。在这些情况下,申办者应咨询审评部门。
B. 弱酸性药物速释制剂
与弱碱性药物相比,业界对弱酸性药物pH依赖性药物相互作用的评价经验相对有限。对于在pH 1~2条件下溶解度低、pH升高后溶解度增大的弱酸性药物,联用质子泵抑制剂(PPI)或H2受体阻滞剂时,可能导致其吸收速率加快、吸收程度增加(表现为血药峰浓度Cmax或血药浓度-时间曲线下面积AUC升高)。但基于目前已上市弱酸性药物的数据,其pH依赖性药物相互作用的幅度通常较小。是否需要开展临床研究,取决于该弱酸性药物的安全性特征,以及剂量/暴露量-安全性相关性。
C. 缓控释制剂
具有 pH 依赖释放机制的缓释制剂、迟释制剂,也存在与抑酸药发生药物相互作用的风险。目前针对该类缓控释制剂的临床 pH 依赖性药物相互作用评价经验十分有限。
若药物为存在 pH 依赖性药物相互作用风险的缓控释剂型,申办方应与对应审评部门沟通咨询。
三、临床DDI研究的设计与实施
• 研究人群:一般而言,为评估酸抑制剂(ARAs)引起的相互作用风险,可在健康受试者中开展专门研究。但出于安全性考虑,某些药物(如细胞毒性药物)不适合在健康受试者中进行研究。此时,应在拟开发该研究药物的目标患者人群中开展研究。DDI研究的受试者例数应足以可靠评估相互作用的程度及其变异性。
• 研究设计:为减少受试者间变异,优先推荐采用交叉设计(固定序列或随机交叉)。若药物半衰期较长,可考虑采用平行设计。
• ARA的选择:DDI研究中ARA及其给药方案的选择,应基于研究目的确定,例如评估最不利情形,或识别合适的风险缓解策略(如错峰给药)。在目前已批准的ARA中,质子泵抑制剂(PPIs)对胃内pH的影响持续时间较长,因此建议研究中采用或至少纳入一种 PPI。如有需要,也可选择其他类别的ARA作为替代进行评估。以下对相关考虑作进一步说明。
♢ PPIs:在给予研究药物前,应先连续给予PPI数日(如4~7天),以使PPI达到药效学稳态。PPI对胃内pH的影响持续时间较长,因此错峰给药,通常不能降低DDI风险。PPI对胃内pH的影响(如24小时平均pH、24小时内pH≥4的时间占比)取决于具体PPI品种及其剂量。优先选择预计可使胃内pH升高接近最大效应的PPI及其剂量。
♢ H2受体阻滞剂(H2 blockers):一般而言,在研究药物给药前给予单次或多次H2受体阻滞剂(如提前2小时),可最大化其升高胃内pH的作用。与PPI相比,H2受体阻滞剂引起的胃内pH升高持续时间较短。因此,对于某些药物,通过错峰给药,可能降低或避免pH依赖性DDI风险。例如,可在H2受体阻滞剂给药前2小时和给药后10~12小时给予研究药物,以降低风险。该策略应通过临床研究加以确认。
♢ 抗酸药(Antacids):可采用单次合并给予抗酸药进行研究,因为其可直接中和胃酸。
♢ 其他考虑:选择用于研究的ARA时,还应考虑除胃内pH变化之外的其他相互作用机制。例如,奥美拉唑已知可抑制CYP2C19;西咪替丁可抑制多种CYP酶和转运体(如CYP2D6、CYP3A4、MATE1和MATE2/K)。因此,优先选择不具有其他相互作用机制的ARA。此外,若预计研究药物会影响某一ARA的PK,则该ARA不应在DDI研究中使用。
• 剂量:为评估最不利情形,申办方应在DDI研究中选择临床实践中常用的ARA最高剂量(例如:艾司奥美拉唑40 mg;奥美拉唑40 mg;泮托拉唑40 mg),同时,建议采用拟用于治疗的研究药物最高推荐剂量,因为该剂量通常更容易受到pH依赖性DDI的影响。如拟采用其他剂量或给药方案,申办方应提供充分论证。
• 制剂:pH依赖性DDI的影响可能与制剂有关。因此,建议使用研究药物的拟上市制剂开展专门研究。需要注意的是,在药物开发早期,拟上市制剂可能尚未确定。若使用早期制剂开展研究,申办方应说明理由,并证明pH依赖性DDI的研究结果可外推至拟上市制剂。
• 研究药物给药频次:一般可接受研究药物采用单次给药,除非多次给药后药物吸收特征发生变化,或研究必须在患者中开展,且对需要持续治疗的患者而言,单次给药无临床获益。
• 进食条件:若研究药物拟空腹服用,则研究应在空腹条件下进行。若研究药物拟不受食物影响服用,也应在空腹条件下进行,因为这通常代表最不利情形。若研究药物拟随餐服用,则研究应在进食条件下进行,且进食条件应与后期临床试验保持一致。需要注意的是,与其他类型食物相比,高脂餐可能低估ARA的pH依赖性DDI影响,因为高脂餐较其他餐食更容易升高基线胃内pH,同时可刺激更多胆汁酸分泌,从而促进药物溶解。
• 药代动力学(PK)采样与数据收集:PK采样时间点应足以充分表征以下参数:AUC₀–∞(多次给药研究中为稳态 AUC0–τ), Cmax, Tmax,如具有临床相关性,还应包括Cmin或部分AUC。以上参数应分别在研究药物单独给药以及与ARA合并给药时进行评估。如果活性代谢产物对研究药物的疗效或安全性有影响,申办方还应测定其浓度。
四、pH依赖性DDI的替代评估方法
• 群体药代动力学(PopPK)分析:
可在临床试验中通过PopPK分析评估研究药物与ARAs之间的DDI。以下补充说明与ARA相关的特殊考虑:
♢ 给药信息记录:pH依赖性DDI的影响对研究药物相对于ARA的给药时间非常敏感(如H2受体阻滞剂或抗酸药)。此外,ARA剂量以及进食情况也可能影响相互作用程度。因此,必须预先制定方案,确保准确记录以下关键信息:
♦ 研究药物和ARA的剂量
♦ 给药时间
♦ 给药持续时间
♦ 进食状态及食物类型(如空腹、高脂餐、普通餐或清淡餐)
♢ PK采样:pH依赖性DDI通常会影响药物吸收。因此,在研究药物吸收阶段设置足够的血样采集时间点非常重要,以更好地捕捉潜在的DDI效应。
♢ 数据分析:由于PPI、H2受体阻滞剂和抗酸药升高胃内pH的持续时间不同,因此应按类别分别评估这些ARA。例如,可将PPI、H2受体阻滞剂和抗酸药分别作为3个独立协变量。如条件允许,还可比较以下两类患者的药物系统暴露:
▷ 在整个试验期间持续使用ARA的患者
▷ 在试验期间间断使用ARA的患者
• 基于生理的药代动力学(PBPK)模拟:结合图1所示的评估框架,PBPK模拟在某些情况下可进一步评估pH依赖性DDI的风险。PBPK方法也可用于指导临床研究设计。如申办方拟采用PBPK模拟评估pH依赖性DDI,建议与相应审评部门进行沟通。
五、临床DDI研究结果的外推
• 一般而言,专门DDI研究中观察到的“研究药物+某一种ARA”的结果,可外推至同类别的其他ARA。例如,某一PPI的研究结果,可外推至其他能够达到相似胃内pH升高效应剂量水平的PPI。• 但如果专门DDI研究所选用的ARA除改变胃内pH外,还具有其他相互作用机制,则将该结果外推至同类其他ARA时,可能受到混杂因素影响。
• 下文提供了一个外推框架,用于将专门研究结果转化为说明书建议。该框架以“弱碱性、速释制剂的研究药物与PPI联合使用”为示例(见图2)。如申办方拟采用其他策略评估pH依赖性DDI,建议与相应审评部门沟通。
• 一般而言,由于PPI对胃内pH的影响持续时间较长,因此在pH依赖性DDI评估中,PPI通常代表最不利情形。因此,如果研究药物与PPI的专门研究结果为阴性,通常可认为该研究药物不存在pH依赖性DDI。研究中的PK变化是否具有临床意义,应结合研究药物的暴露-反应关系进行判断,例如对疗效或安全性的影响。
• 如果研究药物与PPI联合用药的研究显示,研究药物暴露发生了具有临床意义的变化,则FDA对风险缓解策略及进一步研究提出以下建议,以优化DDI风险管理:
♢ PPIs:应避免该药物与PPI合用。作为替代方案,申办方可考虑开展额外研究,评估较低剂量PPI的影响。
♢ H2受体阻滞剂:应避免该药物与H2受体阻滞剂合用。作为替代方案,申办方可针对研究药物开展额外研究,评估一种或多种错峰给药方案,以确定在临床实践中可行、且能够降低pH依赖性DDI风险的给药方案。
♢ 抗酸药:由于抗酸药作用时间较短,可通过与其错峰给药来降低风险。例如,可在使用抗酸药前2小时或后2小时给予研究药物。如有需要,申办方可进一步开展研究,评估研究药物与抗酸药更短间隔错峰给药的可行性。
上述风险缓解策略应在说明书中予以适当体现。
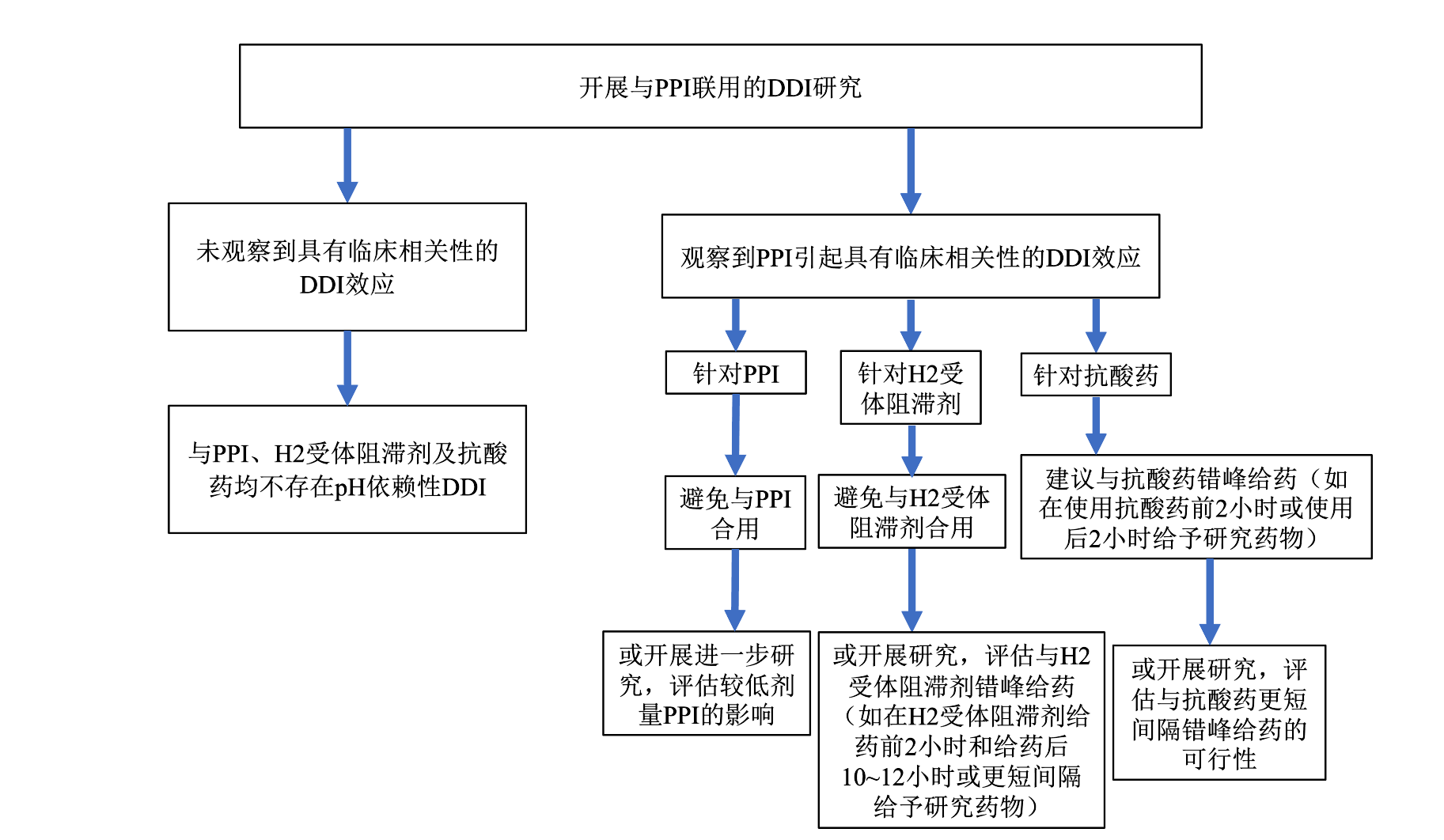
图2. 弱碱性药物速释制剂临床DDI研究结果的外推及其意义
六、说明书建议
处方信息必须包含医疗卫生专业人员安全、有效使用该药物所需的关键科学信息摘要。撰稿人:Frances Zhao, Henry Liu
